张颖 诺华创新药物中国总裁 诺华创新药物(中国)总裁张颖表示:“乳腺癌是威胁女性健康的第一大肿瘤,也是诺华关注和探索的重点领域之一。我非常高兴凯丽隆®成为了中国首个获批用于晚期一线绝经前乳腺癌适应症的CDK4/6抑制剂。这是凯丽隆®在中国获批的第一个适应症,相信将为中国乳腺癌患者,尤其是绝经前的乳腺癌患者带来新的治疗方案和新的希望。秉承‘以患者为中心’的理念,诺华将持续带来高价值的创新药物,引领乳腺癌治疗发展,并促进创新药物的可及性,从而使更多患者获益。”
据世界卫生组织国际癌症研究机构发布的2020年全球最新癌症数据,全球乳腺癌新发病例高达226万例,已取代肺癌成为全球第一大癌种[1]。
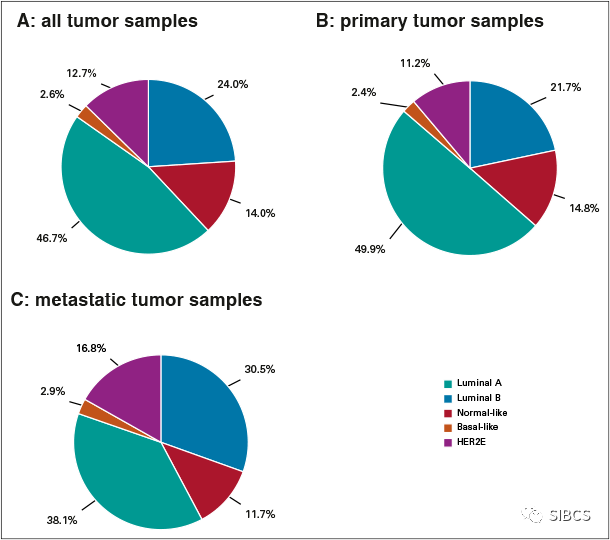
在中国,乳腺癌是女性常见的恶性肿瘤之一,发病率位居女性恶性肿瘤之首[2,3]。而这个群体中,有约70%的患者为HR+/HER2-乳腺癌[4]。疾病的复杂性给这类晚期乳腺癌治疗带来了巨大挑战,亟需创新的治疗方式。
内分泌治疗是HR+/HER2-晚期乳腺癌经典的系统性治疗手段,然而,仍然有患者难免会出现原发或继发耐药[5],使得内分泌治疗疗效大打折扣。随着内分泌治疗联合分子靶向治疗的开展,CDK4/6抑制剂越来越成为其中的“重头戏”。
徐兵河 教授
中国工程院院士
中国医学科学院肿瘤医院
药物临床试验研究中心(GCP)主任
中国工程院院士、中国医学科学院肿瘤医院药物临床试验研究中心(GCP)主任徐兵河教授指出:“中国乳腺癌发病率年增长速度是世界平均水平的2倍,并且初诊时绝经前患者约占60%[6]。因此,迫切需要更加适合国内患者疾病特征的治疗方案。我很高兴看到凯丽隆®在国内获批,该药的获批将为我国绝经前晚期乳腺癌患者提供更多治疗选择,并有望进一步延长晚期患者生存期以及改善患者生活质量。”
凯丽隆®是拥有最大规模临床试验证据的CDK4/6抑制剂。MONALEESA全球研究包括诺华申报的三项试验,其中MONALEESA-7研究结果提示,与内分泌治疗相比,凯丽隆®+内分泌治疗作为绝经前HR+/HER2-晚期乳腺癌(ABC)患者的初始治疗,无进展生存期(PFS)和总生存期(OS)具有统计学的显著获益[7,8]。
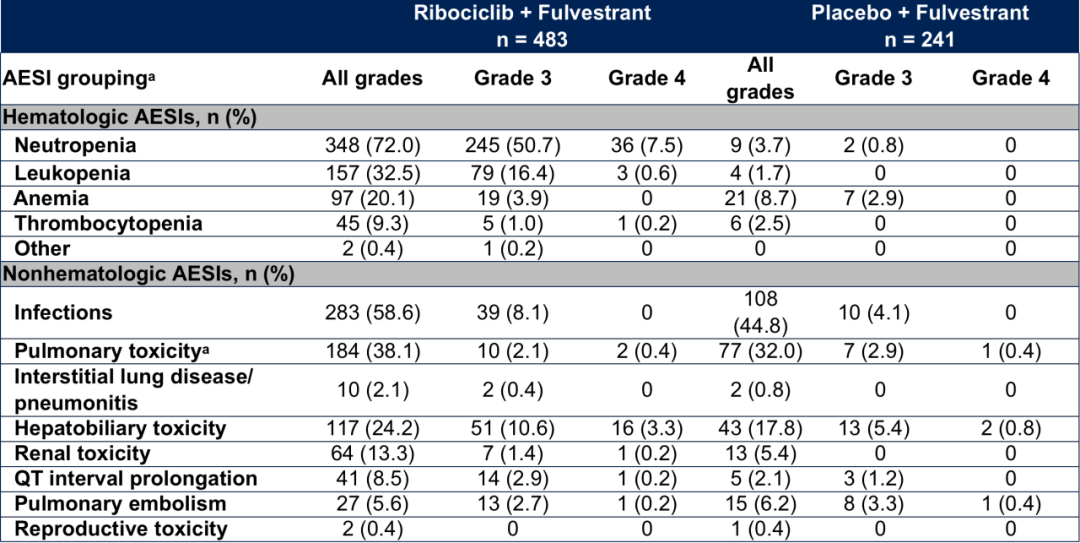
本次获批是基于在中国进行的一项临床试验,研究结果显示,无论患者绝经状态如何,与安慰剂+内分泌治疗相比,凯丽隆®+内分泌治疗均显示无进展生存期(PFS)获益和良好的安全性特征,总体安全性特征与凯丽隆®的已知不良反应相似,与MONALEESA全球研究保持一致。
邵志敏 教授
复旦大学附属肿瘤医院
该临床试验的主要研究者
该临床试验的主要研究者、复旦大学附属肿瘤医院邵志敏教授表示:“我国乳腺癌患者的发病高峰在45-55岁,相对绝经后,绝经前乳腺癌更具有侵袭性。延长生存期和改善生活质量一直是晚期乳腺癌治疗的目标之一。我们在中国进行的相关临床试验和MONALEESA全球研究均提示,凯丽隆®联合内分泌治疗,与内分泌单药治疗相比,具有卓越的总体生存获益。我们希望能够尽快应用于临床,为更多绝经前乳腺癌患者带来新希望。”
一直以来,诺华在全球深耕乳腺癌治疗领域,从已上市多年的弗隆®、飞尼妥®,到最新获批的凯丽隆®以及未来即将引入中国市场的Alpelisib,诺华期望通过不断开发并推出前沿创新药物,带给乳腺癌患者更多生命尊严和信心,让她们在延长生命长度的同时还能享受到更有质量的生活,点燃她们的生命之光!